Un nouveau mode d’action de l’ellipticine, une molécule connue pour ses propriétés anticancéreuses vient d’être identifié par des chercheurs du CEA(1), du CNRS, de l’Inserm, de l’Institut Curie et de l’Université Joseph Fourier-Grenoble 1. Ils ont sélectionné des dérivés de cette molécule capable de cibler spécifiquement la protéine CK2, une protéine-kinase(2) dérégulée dans de nombreux cancers, et ont mis en évidence le potentiel anti-tumoral de ces dérivés. Ces travaux, publiés en ligne par la revue Cancer Research, ouvrent des perspectives nouvelles pour la conception de futurs médicaments anticancéreux.
L’ellipticine est une molécule isolée en 1959 à partir des feuilles d’Ochrosia elliptica, une plante alcaloïde commune en Océanie. En raison de leur forte activité anti-tumorale, l’ellipticine et ses dérivés ont très tôt fait l’objet de recherches en cancérologie afin de mettre au point de nouveaux médicaments. Utilisées pour le traitement de patients, ces molécules se sont cependant avérées responsables d’effets secondaires importants, ce qui a abouti à l’arrêt de leur utilisation. Des études ont montré que leur mécanisme d’action est peu sélectif. Leurs propriétés anti-tumorales reposent en effet sur leur capacité à provoquer des cassures dans l’ADN. Cependant, des résultats récents ont montré que certains dérivés de l’ellipticine avaient un mode d’action beaucoup plus ciblé, agissant spécifiquement sur des protéine-kinases. Les protéine-kinases sont des composants majeurs dans la propagation de signaux contrôlant la prolifération et la survie des cellules. Le dysfonctionnement de certaines de ces kinases est associé au développement de cancers. C’est le cas notamment de la protéine-kinase CK2, hyperactive dans de nombreux cancers, notamment ceux du sein et de la prostate.
D’où l’idée des chercheurs du CEA, du CNRS, de l’Inserm, de l’Institut Curie et de l’Université Joseph Fourier de cribler les 6 560 molécules de la chimiothèque de l’Institut Curie, à la recherche de dérivés de l’ellipticine ciblant spécifiquement la protéine-kinase CK2. Ils ont ainsi trouvé des inhibiteurs dont le mode d’action est lié à la parfaite adéquation entre leur forme et le site actif de CK2 dans lequel ils viennent se placer. Ces inhibiteurs sont non seulement capables d’empêcher la prolifération des cellules in vitro, mais leur potentiel anti-tumoral a été confirmé chez la souris. « Avec ces résultats, nous avons mis en évidence un nouveau mécanisme d’action pour certains dérivés de l’ellipticine », s’enthousiasme Claude Cochet, responsable de l’équipe Structure et fonctions cellulaires de la protéine-kinase CK2 labellisée par la Ligue Nationale contre le Cancer. « Ces composés inhibent fortement la protéine-kinase CK2 et bloquent ainsi la progression tumorale. Du fait de leur mode d’action très sélectif, ils sont particulièrement actifs et présentent un risque d’effets secondaires beaucoup plus faible ».
Récemment et pour la première fois, un essai clinique vient d’être lancé aux États-Unis pour tester l’utilisation potentielle d’inhibiteurs de la protéine-kinase CK2 dans la lutte contre le cancer. Dans ce contexte, les dérivés de l’ellipticine ciblant CK2, développés par les chercheurs français, s’avèrent eux aussi très prometteurs pour le traitement des cancers associés à un dysfonctionnement de la protéine-kinase CK2.
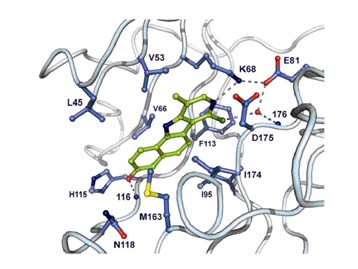
Cette structure cristallographique montre comment un dérivé de l'ellipticine inhibe la protéine-kinase CK2. La structure plane de cette molécule chimique lui permet de s'engager dans le site catalytique et de prendre la place du substrat de l'enzyme. Les acides aminés de la CK2 sont en bleu et le dérivé de l'ellipticine en vert. © CEA
Notes :
(1) Équipe Structure et fonctions cellulaires de la protéine kinase CK2 (Inserm/CEA) et Centre de criblage pour des molécules bioactives de l’Institut de recherche en technologie et sciences pour le vivant. Laboratoire de cristallographie et de cristallogenèse des protéines de l’Institut de biologie structurale J.P. Ebel (CEA/CNRS/Université Joseph Fourier).
(2) Les protéine-kinases sont des enzymes qui jouent un rôle important dans la propagation de signaux qui permettent à la cellule de contrôler sa prolifération et sa survie.
Références :
Antitumor activity of pyridocarbazole and benzopyridoindole derivatives that inhibit protein kinase CK2. Renaud Prudent, Virginie Moucadel, Chi-Hung Nguyen, Caroline Barette, Frédéric Schmidt, Jean-Claude Florent, Laurence Lafanechère, Céline F. Sautel, Eve Duchemin-Pelletier, Elodie Spreux, Odile Filhol, Jean-Baptiste Reiser, and Claude Cochet. Cancer Research, online, 2010
Référence des équipes :
Institut de biologie structurale J.P. Ebel, UMR 5075 CEA/CNRS/Université Joseph Fourier, Grenoble –
Laboratoire de cristallographie et de cristallogenèse des protéines.
Institut de recherches en technologies et sciences pour le vivant (iRSTV, Grenoble) – Laboratoire de transduction du signal, UMR U873-CEA/Inserm/Université Joseph Fourier.
Institut de recherches en technologies et sciences pour le vivant (iRSTV, Grenoble) – Centre de criblage pour des molécules bioactives.
UMR 176 CNRS-Institut Curie, Orsay-Paris
Source: communiqué de presse du CNRS
Laisser un commentaire